Ricerca sull’invecchiamento definita: Le 12 cause dell’invecchiamento

Indice dei contenuti
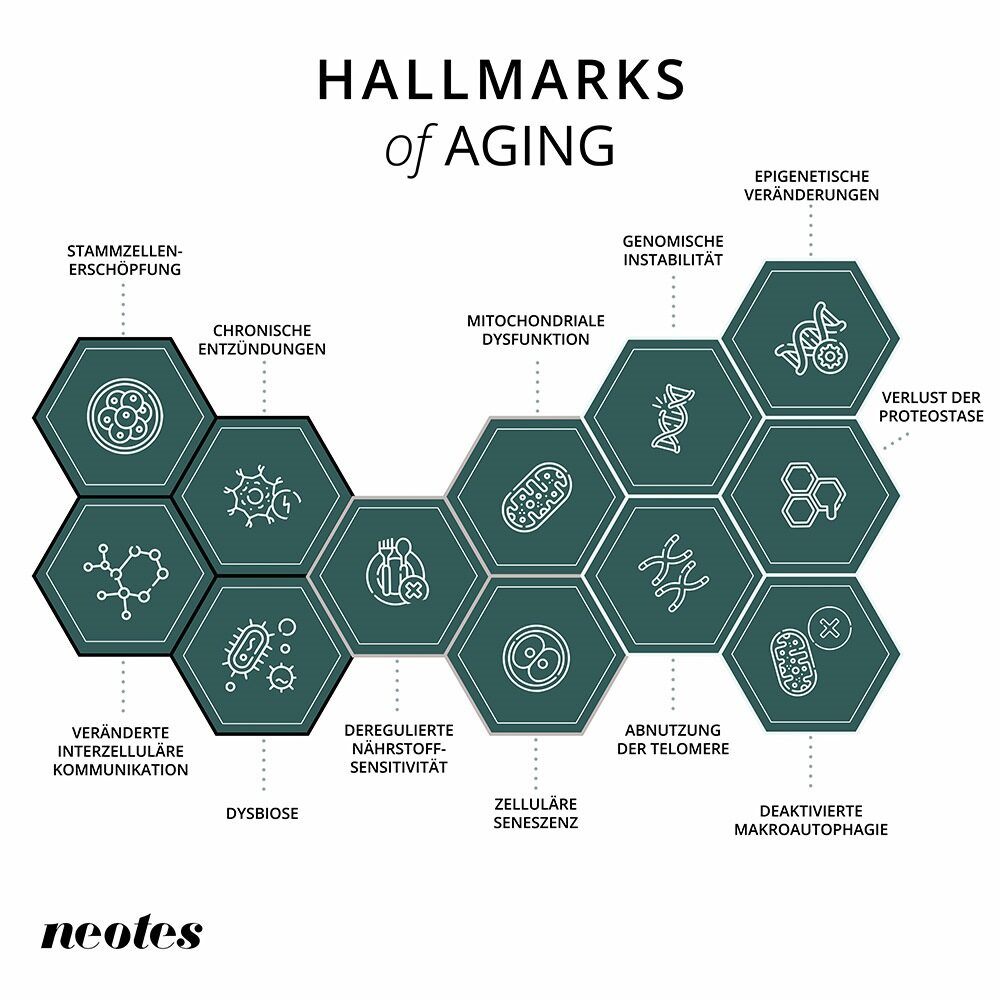
L’invecchiamento del corpo consiste in una serie di processi interconnessi. La recente ricerca biomedica ha portato allo sviluppo dei ”segni distintivi dell’invecchiamento”, i processi che controllano il processo di invecchiamento a livello cellulare.
1. cambiamenti epigenetici
Il nostro genoma è costituito da lunghi filamenti di DNA avvolti da bobine proteiche (istoni). Questi istoni sono dotati di dispositivi chimici che supportano l’accensione e lo spegnimento dei geni. Questi dispositivi di accensione formano il cosiddetto epigenoma. L’epigenoma si modifica con l’età e ciò può compromettere il buon coordinamento dell’attività genica. Le sirtuine sono un gruppo particolarmente studiato di enzimi che influenzano l’epigenoma. Tuttavia, anche la dieta, i farmaci o le modifiche dello stile di vita possono alterare l’epigenoma.
2. perdita della proteostasi
Il compito principale dei geni è quello di produrre proteine. Queste regolano praticamente tutte le reazioni chimiche della cellula e devono essere ripiegate in forme precise per poter svolgere il loro compito. In età avanzata, a causa di danni epigenetici, si verifica un ripiegamento errato, a seguito del quale le proteine non svolgono più il loro compito. Il processo che regola il mantenimento di tutte le proteine nella loro forma originale è chiamato proteostasi.
3. autofagia disattivata
L’autofagia è un processo delle nostre cellule che scompone i componenti cellulari danneggiati o non funzionanti e li riutilizza. Un meccanismo di riciclo, per così dire. Questa funzione è essenziale per mantenere la salute delle cellule e proteggere dall’accumulo di sostanze tossiche. L’autofagia diminuisce con l’età, il che significa che i ”rifiuti” cellulari, come le proteine o gli organelli danneggiati, non vengono più eliminati completamente. Questo favorisce lo sviluppo di malattie legate all’età, come quelle neurodegenerative o il cancro.
4. misurazione dei nutrienti deregolamentata
Se il corpo è ricco di nutrienti, le cellule si moltiplicano. Tuttavia, se questi scarseggiano, l’organismo si concentra sulla manutenzione e sulla riparazione. Sono stati sviluppati studi per simulare la carenza di nutrienti nell’organismo con l’aiuto della riduzione degli alimenti e/o dei farmaci. Queste strategie hanno migliorato la salute e la longevità negli esperimenti sugli animali.
5. disfunzione dei mitocondri
I mitocondri sono le ”centrali elettriche della cellula”, ma producono anche radicali liberi (specie reattive dell’ossigeno o ROS) che danneggiano le cellule. Una nuova linea di pensiero suggerisce che i radicali dell’ossigeno potrebbero essere importanti nel segnalare lo stress cellulare, inducendo le cellule, gli organi e i tessuti ad aumentare i processi di manutenzione e riparazione.
6. senescenza cellulare
La senescenza cellulare è un fenomeno in cui le cellule smettono di dividersi. Con l’avanzare dell’età, queste cellule invecchiate si accumulano e rilasciano segnali nocivi nell’ambiente. La causa della senescenza cellulare è l’accorciamento dei telomeri, componenti del DNA nei cromosomi che sono importanti per tutti i processi biologici. Sono associati all’invecchiamento.
Un recente lavoro in cui i topi sono stati geneticamente modificati in modo che i ricercatori potessero eliminare molte delle loro cellule senescenti, ha mostrato evidenti benefici per la salute, tra cui una maggiore durata della vita. Attualmente si sta lavorando per identificare farmaci che mirino all’eliminazione delle cellule senescenti.
7. esaurimento delle cellule staminali
La capacità del nostro corpo di rigenerare tessuti e organi dipende da cellule staminali sane. Esse sono in grado di differenziarsi in diversi tipi di cellule e di replicarsi in base alle necessità. Con l’avanzare dell’età, le riserve di cellule staminali si esauriscono o le cellule staminali che invecchiano non funzionano più bene.
8. alterazione della comunicazione intracellulare
La comunicazione tra cellule e tessuti è essenziale per il mantenimento delle funzioni corporee. Gli ormoni, ad esempio, sono importanti messaggeri per la comunicazione cellulare. L’infiammazione cronica legata all’età, presumibilmente a causa delle cellule senescenti, può ridurre o interrompere significativamente la comunicazione. Il ripristino di una corretta comunicazione intracellulare potrebbe migliorare la salute, ad esempio riducendo l’infiammazione cronica legata all’età.
9 Infiammazione cronica
L’infiammazione cronica è un’altra caratteristica dell’invecchiamento, caratterizzata da reazioni infiammatorie persistenti in tutto l’organismo. A differenza dell’infiammazione acuta, che garantisce una difesa rapida ed efficace contro minacce come le infezioni, l’infiammazione cronica rimane attiva per un lungo periodo di tempo. Spesso è innescata da fattori legati all’età, come cellule senescenti, DNA danneggiato o mitocondri disfunzionali. Questi processi infiammatori possono portare a un deterioramento della funzione delle cellule e dei tessuti e aumentare il rischio di malattie legate all’età come l’Alzheimer, il diabete e le malattie cardiovascolari.
10. disbiosi del microbioma
Il microbioma, che si trova nell’intestino umano, svolge un ruolo particolarmente importante per la nostra salute e per il processo di invecchiamento. Più invecchiamo, più la composizione della nostra flora intestinale cambia. Questo processo è noto come disbiosi. Questo cambiamento può indebolire il sistema immunitario, favorire l’infiammazione cronica e compromettere l’assorbimento dei nutrienti. La disbiosi è anche associata a malattie legate all’età come il diabete, le malattie cardiache e i disturbi neurodegenerativi.
11. instabilità genomica
Il genoma, ovvero il materiale genetico di un organismo vivente, è responsabile del buon funzionamento di tutte le funzioni corporee. Gli agenti inquinanti esterni o interni, come l’inquinamento o i radicali liberi, danneggiano costantemente il DNA delle nostre cellule; i processi di riparazione cellulare possono riconoscere e compensare questi danni. Con l’avanzare dell’età, i danni al genoma si accumulano e i processi di riparazione non riescono più a tenere il passo. Il cancro è una conseguenza dei danni al DNA non riparati. Gli organismi viventi con processi di riparazione del DNA compromessi mostrano segni di invecchiamento accelerato.
12. accorciamento dei telomeri
L’attrito dei telomeri è un particolare tipo di instabilità genomica. I telomeri sono sequenze ripetitive di DNA che proteggono le estremità dei cromosomi e impediscono che vengano confusi con filamenti di DNA rotti. I telomeri determinano la nostra durata di vita e vengono accorciati dalla normale divisione cellulare, ma anche da processi che danneggiano il DNA. Quando i telomeri raggiungono una lunghezza critica, la replicazione cellulare viene interrotta. La telomerasi, un enzima del nucleo cellulare, può prevenire l’accorciamento dei telomeri e persino ripristinarne la lunghezza.
Fonti:
- Carlos López-Otín, Maria A Blasco, Linda Partridge, Manuel Serrano. I tratti distintivi dell’invecchiamento. Cell. 2013 Jun 6;153(6):1194-1217. doi: 10.1016/j.cell.2013.05.039 .
- https://www.pexels.com/de-de/foto/sonnig-fashion-mode-strand-5263471



